ISSN đang cập nhật


ĐẢM BẢO CHẤT LƯỢNG PEPTIDE DÙNG TRONG ĐIỀU TRỊ
Nguyễn Thị Hồng Hạnh1,4, Trương Ngọc Quỳnh Nhi2, United States Pharmacopeia3
1Trung tâm Đào tạo & Dịch vụ Kiểm nghiệm, Viện KNT TP.HCM
2Khoa Vắc xin & Sinh phẩm, Viện KNT TP.HCM
3United States Pharmacopeia (USP)
4Mạng lưới Phòng thí nghiệm Khối phổ Việt Nam (VMSLN)
Summary
Synthetic therapeutic peptides are gaining prominence as a promising class of drugs, combining the targeted efficacy of biologics with the regulatory advantages of small molecules. However, their development and manufacturing demand rigorous quality control, particularly in the characterization and control of impurity profiles.Guidelines from the USP, along with those from other guideline-developing organizations and regulatory authorities, provide comprehensive frameworks to ensure the efficacy, safety, and quality of peptide-based products.This review highlights key control points essential for ensuring the quality of synthetic therapeutic peptides, including their critical quality attributes, impurity profiles, raw material specifications, and the use of well-characterized reference standards in analytical testing.
Peptide là chuỗi acid amin ngắn, thường dưới 40 acid amin [1] hoặc dưới 5.000 Dalton [2], có vai trò chức năng sinh học quan trọng như điều hòa miễn dịch, truyền tín hiệu nội bào, hay kiểm soát hoạt động nội tiết. Các liệu pháp peptide ngày càng được quan tâm do các ưu điểm như khả năng chọn lọc cao, hiệu quả vượt trội, độc tính thấp, tương thích sinh học tốt, và thời gian bán hủy có thể điều chỉnh thông qua cải tiến hóa học [1,3-4]. Ra đời năm 1963 bởi nhà khoa học đạt giải Nobel Bruce Merrifield, phương pháp tổng hợp peptide pha rắn (SPPS) cho phép tạo ra peptide dài hơn 20 acid amin, là yếu tố then chốt thúc đẩy nghiên cứu peptide. Những năm gần đây, các chiến lược bào chế và gắn kết phân tử mới đã mở ra các đường dùng thay thế và kéo dài thời gian bán thải của các thuốc peptide, từ đó cải thiện khả năng tuân thủ điều trị của bệnh nhân [1]. Kết quả là ngày càng có nhiều thuốc peptide được đưa vào phát triển lâm sàng và phê duyệt.
Bảng 1. So sánh thuốc phân tử nhỏ, peptide, và sinh phẩm (protein/kháng thể) [3-5]
| Phân tử nhỏ | Peptide | Sinh phẩm |
Đặc điểm |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cấp phép/ Đăng ký thuốc tại Hoa Kỳ |
|
|
|
|
|
|
|
Bên cạnh sự phát triển của kỹ thuật tổng hợp và phân tích hiện đại, các tiến bộ sinh học cấu trúc và công nghệ tái tổ hợp cũng góp phần thúc đẩy mạnh mẽ việc phát triển thuốc peptide. Hệ thống phát triển thuốc peptide đã được thiết lập hoàn chỉnh với các bước như: khám phá peptide hoạt tính, thiết kế thuốc, tổng hợp peptide, biến đổi cấu trúc và đánh giá hoạt tính. Tính đến nay, gần 100 thuốc peptide đã được phê duyệt toàn cầu, và không còn giới hạn là hormone tự nhiên hay chuỗi acid amin nguyên thủy. Ví dụ, enfuvirtide là peptide dài 36 acid amin mô phỏng protein virus HIV để dùng kết hợp trong điều trị HIV, còn liraglutide là peptide tổng hợp tương tự GLP-1 có gắn palmitic acid tại K26 thông qua glutamic acid để dùng trong điều trị đái tháo đường type 2. 170 peptide khác đang trong các giai đoạn thử nghiệm lâm sàng, bên cạnh nhiều nghiên cứu tiền lâm sàng trên khắp thế giới [3,4].
Bảng 2. Một số thuốc peptide được phê duyệt từ năm 2000 [4]
Đích (Target) | Tên peptide | Năm phê duyệt đầu tiên | Chỉ định được phê duyệt |
Thụ thể GLP-1 | Exenatide | 2005 | Đái tháo đường type 2 |
Liraglutide | 2009 | ||
Lixisenatide | 2013 | ||
Albiglutide | 2014 | ||
Dulaglutide | 2014 | ||
Semaglutide | 2017 | ||
Thụ thể GLP-2 | Teduglutide | 2012 | Hội chứng ruột ngắn và kém hấp thu |
Thụ thể GC-C | Linaclotide | 2012 | Hội chứng ruột kích thích kèm táo bón và táo bón vô căn mạn tính |
Thụ thể calcitonin | Pramlintide | 2005 | Đái tháo đường type 1 và type 2 |
Thụ thể GnRH | Abarelix | 2003 | Ung thư tuyến tiền liệt giai đoạn tiến triển |
Degarelix | 2008 | ||
Proteasome 20S | Carfilzomib | 2012 | Đa u tủy xương |
Protein NOD2 | Mifamurtide | 2009 | Ung thư xương ác tính |
Thụ thể VIP1 | Aviptadil | 2000 | Rối loạn cương dương |
Thụ thể oxytocin (OT) | Atosiban | 2000 | Trì hoãn chuyển dạ sinh non |
Carbetocin | 2001 | Băng huyết sau sinh | |
Thụ thể TRH | Taltirelin | 2000 | Thoái hóa tiểu não |
Thụ thể melanocortin | Bremelanotide | 2019 | Rối loạn ham muốn tình dục giảm |
Thụ thể PTH1 | Teriparatide | 2002 | Loãng xương |
Abaloparatide | 2017 | ||
Guanylate cyclase C | Plecanatide | 2017 | Táo bón vô căn mạn tính |
Thụ thể NPR-A | Nesiritide | 2001 | Suy tim cấp mất bù |
Thụ thể angiotensin II | Angiotensin II | 2017 | Nhiễm trùng huyết và sốc nhiễm trùng |
Thụ thể beta2 | Icatibant | 2008 | Phù mạch di truyền cấp tính |
gp41 (HIV protein) | Enfuvirtide | 2003 | Điều trị kết hợp HIV-1 |
Thụ thể GHRH | Tesamorelin | 2010 | Giảm loạn dưỡng mỡ ở bệnh nhân HIV |
Kênh canxi type N | Ziconotide | 2004 | Điều trị đau mạn tính nghiêm trọng |
Thụ thể thrombopoietin | Romiplostim | 2008 | Giảm tiểu cầu miễn dịch mạn tính |
Thụ thể erythropoietin | Peginesatide | 2012 | Thiếu máu liên quan đến bệnh thận mạn tính |
Surfactant phổi | Lucinactant | 2012 | Phòng ngừa hội chứng suy hô hấp ở trẻ sơ sinh |
Thụ thể cảm ứng canxi | Etelcalcetide | 2016 | Cường cận giáp thứ phát |
Thụ thể MC1 | Afamelanotide | 2014 | Phòng ngừa phản ứng quang độc |
Thụ thể somatostatin | Pasireotide | 2012 | Hội chứng Cushing |
Thụ thể somatostatin (chẩn đoán) | Lutetium Lu 177 dotatate | 2018 | Khối u thần kinh nội tiết dương tính với thụ thể somatostatin |
Edotreotide Ga-68 | 2019 | Chẩn đoán khối u thần kinh nội tiết | |
Thụ thể melanocortin-4 | Setmelanotide | 2020 | Kiểm soát cân nặng mạn tính do béo phì |
Thị trường thuốc peptide toàn cầu tăng trưởng mạnh. Top 10 thuốc bán chạy nhất năm 2023 bao gồm 7 thuốc trị tiểu đường (Semaglutide – Ozempic và Rybelsus của Novo Nordisk; Dulaglutide – Trulitciy của Eli Lily; Tirzepatide – Mounjaro của Eli Lilly; Insulin/Aspart – NovoRapid của Novo Nordisk; Insulin/Lispro – Humalog của Eli Lilly; Insulin/Glargine – Lantus của Sanofi), 2 thuốc kiểm soát cân nặng (Semaglutide – Wegovy của Novo Nordisk; Liraglutide – Saxenda của Novo Nordisk), và 1 thuốc trị ung thư (Carfilzomib – Kyprolis của AMGEN) [3]. Ước tính về quy mô thị trường năm 2025 giữa các cơ quan nghiên cứu có thể khác nhau, nhưng đều cho thấy xu hướng mở rộng nhanh chóng. Ví dụ, theo Precedence Statistics, thị trường liệu pháp peptide toàn cầu dự kiến sẽ đạt 52,6 tỷ USD vào năm 2025, với tốc độ tăng trưởng kép hàng năm (CAGR) khoảng 5,3% cho giai đoạn 2025 tới 2034. Khu vực Châu Á Thái Bình Dương dự định sẽ tăng trưởng nhanh nhất với CAGR 6,20%. Trong Kế hoạch 5 năm lần thứ 14 của Trung Quốc (2021–2025), phát triển công nghệ y sinh học được coi là lĩnh vực chiến lược quan trọng hàng đầu, trong đó thuốc peptide là một trọng điểm ưu tiên. Vào tháng 1/2024, WuXi AppTec tuyên bố rằng hai cơ sở sản xuất peptide mới tại Trường Châu và Thái Hưng (Trung Quốc) đã chính thức đi vào hoạt động, mở rộng quy mô sản xuất và nâng tổng thể tích bình phản ứng tổng hợp peptide SPPS lên 32.000 lít. Phân khúc thuốc cải tiến (innovative peptide) chiếm tỷ trọng lớn nhất, hơn 60,40% thị phần doanh thu trong năm 2024[6].
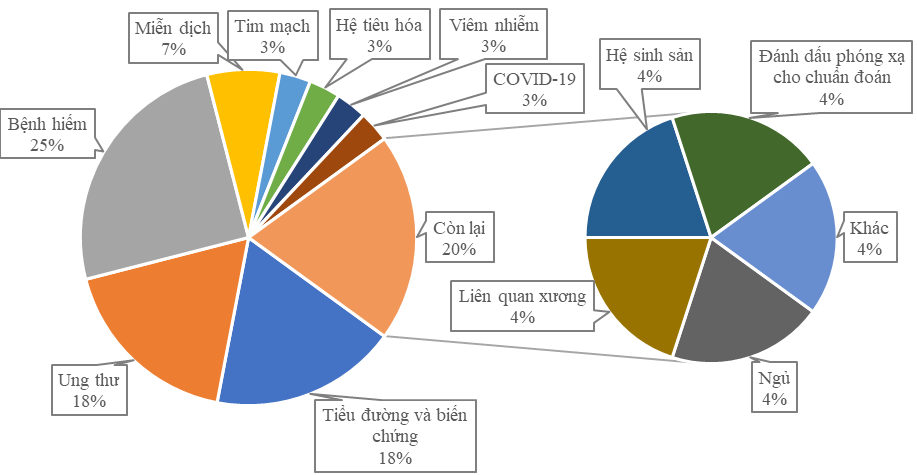
| ||
|
Hình 1. Chỉ định điều trị của thuốc peptide đã được phê duyệt (A) và đang thử nghiệm lâm sàng giai đoạn III (B) [3]
Với sự phát triển của công nghệ và thị trường thuốc peptide, việc thiết lập các tiêu chuẩn chất lượng, phương pháp kiểm nghiệm, cùng với chất chuẩn peptide đi kèm, là cần thiết để đảm chất lượng của sản phẩm trong suốt quá trình phát triển, sản xuất và lưu hành trên thị trường.
Tổng hợp peptide pha rắn (SPPS) là phương pháp phổ biến nhất hiện nay [9]. Trong phương pháp này, chuỗi peptide được gắn cố định trên một resin rắn, cho phép loại bỏ dễ dàng các thuốc thử dư và acid amin chưa phản ứng sau mỗi bước phản ứng. Nhờ vậy, các tạp chất không liên quan đến peptide thường không ảnh hưởng nhiều đến độ tinh khiết của sản phẩm cuối. Tuy nhiên, các tạp chất liên quan đến peptide – phát sinh trong quá trình ghép nối acid amin và loại bỏ nhóm bảo vệ – lại có xu hướng tích lũy dần. Những tạp chất này thường có cấu trúc gần giống peptide đích, khiến hồ sơ tạp chất trở nên phức tạp và khó kiểm soát [1]. Tổng hợp peptide pha lỏng (Liquid-Phase Peptide Synthesis – LPPS) ít được sử dụng hơn và thường áp dụng cho các peptide ngắn. Phương pháp này có tốc độ tổng hợp chậm hơn SPPS, nhưng lại có ưu điểm là dễ kiểm soát tạp chất hơn, do các tạp chất thường có cấu trúc khác biệt rõ rệt so với peptide đích và ít bị tích lũy hơn nhờ khả năng tinh chế tại các bước trung gian [1,9]. Ngoài ra, quy trình tổng hợp kết hợp SPPS và LPPS cũng được áp dụng, trong đó các đoạn peptide ngắn được tổng hợp bằng SPPS, sau đó nối lại với nhau bằng kỹ thuật LPPS để tạo ra peptide dài hơn [9].
Các cơ quan quản lý như Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US FDA) [7] và Cơ quan Dược phẩm Châu Âu (EMA) [8] yêu cầu kiểm soát chặt chẽ chất lượng thuốc peptide nhằm đảm bảo tính an toàn, nhất quán và hiệu quả của sản phẩm. Hình 2 thể hiện các yêu cầu chính trong kiểm soát quy trình sản xuất, kiểm tra đặc tính peptide, thiết lập tiêu chuẩn chất lượng, và đánh giá độ ổn định để đảm bảo chất lượng thuốc peptide tổng hợp [9]. Hướng dẫn của USP, US FDA, EMA đặc biệt nhấn mạnh yêu cầu hồ sơ tạp chất toàn diện, bao gồm tạp chất liên quan đến peptide như biến thể chuỗi, đồng phân, chèn/xóa acid amin, phân hủy [1,7-9]. Nguyên liệu đầu vào cũng phải được kiểm soát chặt chẽ, bao gồm thông tin nhà sản xuất, quy trình tổng hợp, và mức độ tạp chất trong nguyên liệu có thể ảnh hưởng đến hồ sơ tạp chất peptide [8,10].
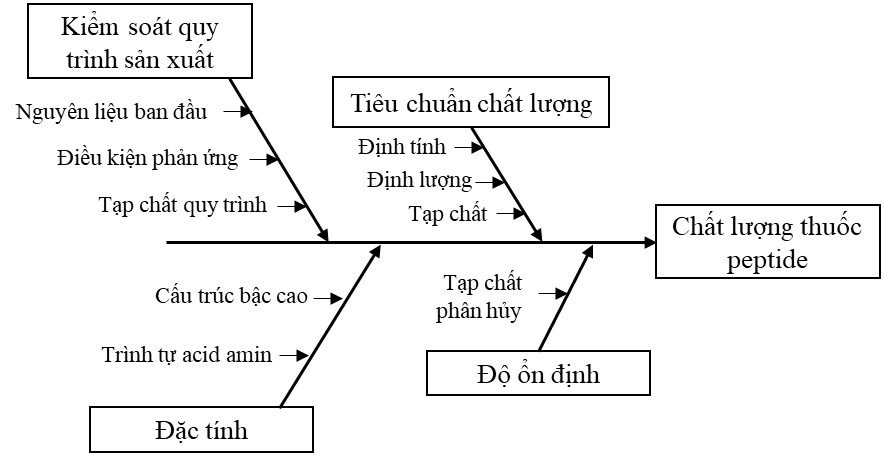
Hình 2. Các yếu tố của chiến lược kiểm soát chất lượng thuốc peptide [9]
2.1. Thuộc tính chất lượng của peptide tổng hợp
Tiêu chuẩn chất lượng của peptide dược chất cần phản ánh các thuộc tính chất lượng quan trọng (CQA) do nhà sản xuất đề xuất và biện minh, đồng thời phải được cơ quan quản lý phê duyệt theo hướng dẫn ICH Q6A và VICH GL39. Việc thiết lập các tiêu chuẩn chất lượng này giúp đảm bảo rằng chất lượng của peptide dược chất được kiểm soát thông qua các thuộc tính như đặc điểm vật lý, định tính, định lượng, mức độ tạp chất, cũng như các phép thử đặc trưng, như được trình bày trong Bảng 3.
Bảng 3. Thuộc tính chất lượng của peptide dược chất theo USP <1053> và các tài liệu khác [1,2,8,11,12]
Thuộc tính | Kỹ thuật/ Phép thử | Chuyên luận USP | Ghi chú [2] |
Tính chất | Kiểm tra bằng mắt | - | - Mô tả ngoại quan dạng rắn và thông tin tính tan nếu có. |
Định tính | HPLC – rửa giải cùng RS | <621> | - Ít nhất 2 phép thử định danh dựa trên tính chất đặc trưng của peptide như kích thước peptide, trình tự chuỗi AA, hồ sơ pI, rửa giải sắc ký, cấu trúc dạng hoạt động. - Ví dụ: Phép thử 1: AAA hoặc NMR; Phép thử 2: RP-LC. Có thể dùng nhiều hơn 1 phép thử RP-LC. - Tiêu chuẩn chấp nhận: dựa trên so sánh với chất chuẩn. |
MS – khối lượng peptide | <736> | ||
Phân tích acid amin (AAA) | <1052>, <507> | ||
MS/MS – chuỗi trình tự | <736> | ||
NMR – chuỗi ít hơn 15 AA | <761> | ||
Sơ đồ chuỗi – chuỗi dài hơn 20 AA | <1055> hoặc MS/MS | ||
Tinh khiết đồng phân – AAA với sắc ký đồng phân và đầu dò MS | <621>, <736> | ||
Phân tích chuỗi N-terminal | Edman degradation | ||
IR – ít dùng | <197>, <854> | ||
Cấu trúc bậc cao | Circular dichroism, NMR, FTIR | ||
Đặc tính sinh học – ít thường quy | <1032>, <1033>, <1034> | ||
Định lượng | HPLC – so sánh với chất chuẩn đối chiếu; có thể dùng cùng phương pháp để định danh và kiểm tạp peptide liên quan | <621> | - Kết quả được tính theo chất khan, không chứa ion đối. - Giới hạn định lượng: Trên: 100% + độ lặp lại cho phép (~2%); Dưới: 100% - độ lặp lại cho phép - hàm lượng tạp chất tối đa cho phép (~4%). |
Cấu phần peptide | AAA | <1052>, <507> |
|
Phân tích nitrogen | <461> | ||
Phổ UV | <197>, <857>, <507> | ||
NMR định lượng (qNMR) | <761>, <1761> | ||
Tạp chất | Tạp peptide liên quan | <621>, LC-MS | Peptide liên quan - Thường sử dụng RP-LC; được thẩm định cho tạp chất đã biết. - Có quy định giới hạn cho: + Từng tạp chất đã định danh + Tạp chất không định danh, thường tại ngưỡng phát hiện + Tổng tạp |
Tồn dư dung môi | <467> | ||
Nguyên tố kim loại | <232>, <233>, <1065> | ||
Tồn dư trifluoroacetic acid | <503.1> | ||
Tồn dư fluoride | <1065> / electrode chọn lọc ion | ||
Tạp chất phân tử nhỏ khác |
| ||
Phép thử khác | Hàm lượng ion đối | <503> cho acetat; <1065> khác | - Chiral chromatography có thể thay thế góc quay cực. - Mất khối lượng do làm khô ít dùng, thường thay bằng xác định hàm lượng nước (Karl Fisher bán vi lượng; chuẩn độ coulometric vi lượng). |
Hàm lượng nước | <921> | ||
Góc quay cực | <781> | ||
Nhóm thiol (-SH) | Ellman’s test | ||
Giới hạn vi sinh | <61>, <62> | ||
Nội độc tố vi khuẩn | <85> |
*Danh mục chữ viết tắt:AA: Acid amin; AAA: Phân tích acid amin; IR: Phổ hồng ngoại; HPLC: Sắc ký lỏng hiệu năng cao; NMR: Cộng hưởng từ hạt nhân; MS: Khối phổ 1 lần; MS/MS: Khối phổ 2 lần; pI: Isoelectric point; RS: Chất chuẩn; RP-LC: Sắc ký lỏng pha đảo.
2.2. Hồ sơ tạp chất toàn diện
Hồ sơ tạp chất của peptide có thể khác biệt đáng kể tùy thuộc vào công nghệ sản xuất được sử dụng.Nhìn chung, các tạp chất liên quan đến peptide có thể phát sinh từ nguyên liệu ban đầu cũng như trong suốt quá trình tổng hợp, tinh chế, đóng gói và bảo quản, như minh họa trong Hình 3.
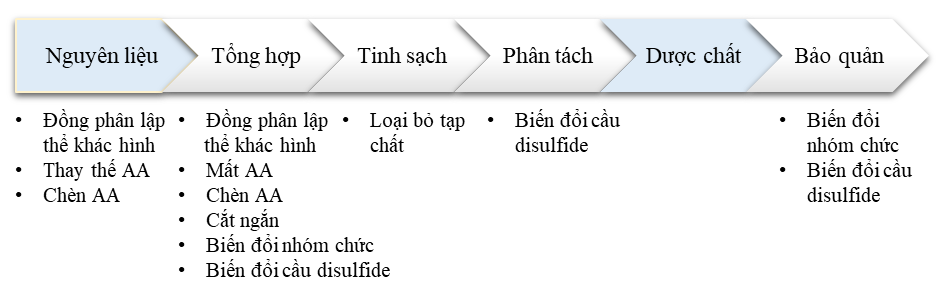
Hình 3. Tổng quan các tạp peptide liên quan [9]
Hồ sơ tạp chất của peptide có thể được phân thành hai nhóm chính: tạp chất liên quan đến peptide và tạp chất không phải peptide. Trong đó, tạp chất liên quan đến peptide thường được kiểm soát nghiêm ngặt hơn và tiếp tục được phân loại thành tạp đã xác định (specified impurities) và tạp chưa xác định (unspecified impurities).Một tạp chất được xem là đã xác định khi giới hạn cho phép của nó đã được đánh giá (qualified) thông qua dữ liệu độc tính, nghiên cứu lâm sàng, hoặc biện luận khoa học dựa trên cấu trúc hóa học.Theo Dược điển châu Âu (Ph. Eur. 2034) [1], tạp chưa xác định phải được kiểm soát ở mức không vượt quá 0,5%, và nếu hàm lượng vượt quá 1,0%, tạp chất đó cần phải được đánh giá đầy đủ (qualified) [9].
Bảng 4. Tổng hợp tạp chất của peptide dược chất theo USP <1053> [1]
Loại tạp | Mô tả | Nguồn gốc | Kỹ thuật |
1. Tạp peptide liên quan | |||
Peptide bị mất acid amin (AA) | Bị loại bỏ một hoặc nhiều AA | Quá trình tổng hợp (ghép nối hoặc khử nhóm bảo vệ không hoàn toàn) hoặc bảo quản (thủy phân đầu N hoặc C của peptide; hoặc phân mảnh) | LC-MS hoặc LC-MS/MS |
Peptide bị chèn AA | Xuất hiện thêm một hoặc nhiều AA | Nguyên liệu (chứa dipeptide tương ứng được bảo vệ) hoặc tổng hợp (mất nhóm bảo vệ đầu N trong quá trình ghép nối) | nt* |
Peptide bị thay thế AA | Thay thế một hoặc nhiều AA | Nguyên liệu (bị nhiễm tạp) hoặc quá trình tổng hợp (các bước rửa không đủ để làm sạch peptide-resin) | LC spike với analogs; phân lập/ AAA/ LC-MS; hoặc LC-MS/MS |
Peptide bị cắt ngắn | Bị mất chuỗi AA đầu N | Nguyên liệu (chứa dư lượng acid acetic); quá trình tổng hợp (cản trở lập thể, gắn nhóm acetyl trong quá trình ghép nối); hoặc bảo quản | LC-MS hoặc LC-MS/MS |
Peptide chứa AA đồng phân | Chứa AA đồng phân lập thể khác hình | Nguyên liệu; quá trình tổng hợp; hoặc bảo quản | LC spike analogs; phân tích chiral |
Peptide chứa biến đổi liên quan Asp hoặc Asn | Chứa aspartimid/ succinimid | Vòng hóa vào mạch chính thông qua mất H2O/NH3 của Asp/Asn | HPLC, LC-MS hoặc LC-MS/MS |
Chứa β-Asp | Mở vòng do thủy phân trung gian aspartimide/ succinimide trong quá trình xử lý hoặc bảo quản | LC spike với analog/ phân tách | |
Có đồng phân Asn | Epime hóa trung gian aspartimide/ succinimide, sau đó mở vòng, trong xử lý hoặc bảo quản | nt | |
Chuỗi bị cắt | Thủy phân hoàn toàn trung gian aspartimide/ succinimide | nt | |
Peptide bị chèn β-Ala | Chuỗi chứa β-Alanine | Nguyên liệu bị nhiễm tạp | LC-MS hoặc LC-MS/MS |
Peptide chứa acid pyro-Glu | Chuỗi chứa Glu hoặc Gln ở đầu N | Quá trình tổng hợp | HPLC hoặc LC-MS |
Oligomers | Chuỗi kết tập hoặc hình thành polymer | Cấu trúc thay đổi hoặc polyme hóa | SEC, SEC-MALS; SV-AUC; DLS; FFF; IMS |
Peptide chứa cầu disulfide | Nhóm thiol (-SH) bị khử | Quá trình tổng hợp hoặc bảo quản | LC-MS hoặc LC-MS/MS |
Peptide tạp khác | Khử amine của Gln, Asn, hoặc đầu C | nt | nt |
Acetyl hóa nhóm amin chức năng | nt | nt | |
Oxy hóa AA chứa vòng benzen hoặc S | Quá trình tổng hợp, bảo quản hoặc chuẩn bị mẫu phân tích | nt | |
Alky hóa, acyl hóa AA | Quá trình loại bỏ bảo vệ (cắt) | nt | |
2. Tạp không phải peptide | |||
Tạp nguyên liệu, trung gian, hóa chất; các sản phẩm phản ứng hoặc phân hủy | Nguyên liệu hoặc hóa chất | <621> HPLC hoặc GC | |
Tồn dư dung môi | Dung môi sử dụng giai đoạn sau của sản xuất (v.d. ACN để rửa giải HPLC tinh sạch) | <467> và ICH Q3C(R7) | |
Tạp vô cơ, tồn dư ion âm của acid hữu cơ, tồn dư ion dương của base | Tồn dư ion âm hoặc ion dương dạng ion đối hoặc thành phần dung dịch đệm (TFA, TEAP, F) | <503>, <503.1>, ICH Q3C(R7) | |
Tạp kim loại | Nguyên liệu, chất xúc tác trong tổng hợp, thiết bị | <232>, <233>, ICH Q3D(R1) | |
Nhiễm vi sinh | Dung dịch nước hoặc đệm ở pH trung tính | <61>,<62>,<1111> | |
Nội độc tố vi khuẩn | Nguyên liệu sử dụng giai đoạn cuối của sản xuất | <85> | |
*nt: Như trên; analogs:có thể hiểu là chuẩn tạp peptide
2.3. Thuộc tính chất lượng của nguyên liệu
Theo USP <1054>, để đảm bảo chất lượng và đáp ứng yêu cầu của cơ quan quản lý, nhà sản xuất peptide dược chất cần thực hiện nghiêm túc công tác đánh giá nhà cung cấp và thẩm định quy trình tổng hợp nguyên liệu đầu vào. Đối với mảnh peptide sử dụng làm nguyên liệu, yêu cầu về độ đồng nhất giữa các lô và khả năng truy xuất toàn bộ công đoạn sản xuất càng nghiêm ngặt. Bất kỳ thay đổi nào trong quy trình tổng hợp các dẫn xuất amino acid (Protected Amino Acid Derivatives – AAD) được bảo vệ đều có thể ảnh hưởng đến chất lượng peptide thành phẩm, do đó, nghĩa vụ của nhà cung cấp trong việc kịp thời thông báo những thay đổi này cần được quy định rõ ràng và giám sát chặt chẽ. Mức độ đánh giá tác động của thay đổi trong quy trình sản xuất nguyên liệu đối với thuộc tính chất lượng của peptide phụ thuộc vào bản chất của nguyên liệu đầu vào – bao gồm acid amin tự do, AAD được bảo vệ, hoặc mảnh peptide [10].
Thuộc tính chất lượng của nguyên liệu bao gồm ngoại quan, định tính, tạp chất, định lượng, và các yêu cầu khác. Trong đó, đáng quan tâm nhất là tạp chất, đặc biệt là tạp chất của AAD. Quy trình tổng hợp AAD có thể phát sinh ba nhóm tạp chất chính: (i) Tạp AAD liên quan có nguồn gốc từ acid amin ban đầu, (ii) Tạp AAD liên quan có nguồn gốc từ quá trình tổng hợp, (iii) Tạp không liên quan đến AAD (dung môi, kim loại, nitrosamines,…). Nhóm tạp thứ nhất có thể ảnh hưởng nghiêm trọng đến độ tinh khiết của peptide dược chất, nhấn mạnh yêu cầu về độ tinh khiết cao của nguồn AA ban đầu. Nhóm tạp thứ hai có thể tác động đáng kể đến hồ sơ tạp chất của sản phẩm. Nhóm thứ ba tuy thường không ảnh hưởng đến phản ứng tổng hợp peptide pha rắn, nhưng vẫn cần được đánh giá đầy đủ về nguy cơ an toàn và ảnh hưởng đến sức khỏe người dùng [10].
Bảng 5. Tạp chất của dẫn xuất acid amin (AAD) theo USP <1054> [10]
Tạpcủa AAD | Nhận xét |
1. Tạp AAD liên quan có nguồn gốc từ acid amin ban đầu | |
AA đối hình gương | Trong 20 amino acid tự nhiên, 19 có đối hình gương; glycine là ngoại lệ do không có carbon bất đối. Dạng S thường được dùng trong tổng hợp peptide vì phổ biến trong tự nhiên và dễ đạt độ tinh khiết quang học cao (<0,1%–0,5% tạp đối hình). Ngược lại, R-amino acid hiếm và khó đạt độ tinh khiết tương đương. |
AA đồng phân lập thể không đối hình | Isoleucine và threonine tồn tại dưới bốn đồng phân lập thể: hai enantiomer (SS và RR) và hai diastereomer (SR và RS). |
AA lạ | Amino acid thường có nguồn gốc tự nhiên và cần trải qua bước phân lập. Trong quá trình này, có thể xảy ra lẫn tạp amino acid khác, chẳng hạn như isoleucine lẫn trong leucine. |
2. Tạp AAD liên quan có nguồn gốc từ quá trình tổng hợp | |
AA bảo vệ không hoàn toàn/ không bảo vệ | Đến từ quá trình sản xuất AAD hoặc phân hủy trong lưu trữ/ vận chuyển. Có thể được loại bỏ dễ dàng nếu tính chất phân cực khác AAD.
|
Tạpβ-Alanine | Nếu sử dụng FMOC-Succinimide làm thuốc thử, có thể dẫn tới tạp FMOC-β-Ala và FMOC-β-Ala-acid amin; cần kiểm soát độ tinh khiết của AAD và/hoặc kiểm soát hàm lượng FMOC-β-Ala và FMOC-β-Ala-acid amin thông qua RP-HPLC hoặc LC-MS với chất chuẩn phù hợp. |
Tạp quy trình khác | Các tạp quy trình khác, ví dụ như dipetide hoặc dẫn xuất AAD khi dùng FMOC-chloride làm thuốc thử. Có thể kiểm soát bằng HPLC và LC-MS; giới hạn chấp nhận phụ thuộc vào khả năng sinh tạp và độ khó loại bỏ. |
3. Tạp không liên quan đến AAD | |
Tồn dư dung môi và thuốc thử |
|
Kim loại | Thường dễ loại bỏ trong SPPS nhưng vẫn cần đánh giá rủi ro để đảm bảo tuân thủ ICH Q3D, USP <232>, <233>. |
Tồn dư chất dị ứng và melamine | Thường ít ảnh hưởng, có thể mua nguyên liệu AA không chứa tồn dư dị ứng (có nguồn gốc từ thực vật gây dị ứng như đậu nành, lúa mạch, lúa mì, ngô) và melamine. |
Prions | AA có nguồn gốc từ động vật hoặc người nên tránh. Yêu cầu nguyên liệu không chứa prion gây bệnh TSE/BSE cần được đưa vào tiêu chí đánh giá và cam kết của nhà cung ứng |
Nitrosamines và tạp gây độc tính gen khác | Tạp N-nitrosamine có thể hình thành khi có mặt đồng thời của tác nhân nitros hóa (như muối nitrit, acid nitrous, ion nitro hóa, nitrosyl halide, nitrosothiol, alkyl nitrite...) và amin bậc hai hoặc ba. Cần tránh các quy trình có nguy cơ tạo nitrosamine. Các tạp chất gây độc gen khác cũng cần được xem xét và đánh giá theo ICH M7. |
Chất chuẩn đóng vai trò thiết yếu trong việc đánh giá các thuộc tính chất lượng của peptide điều trị. Vì chất chuẩn là vật liệu thực tế được sử dụng để kiểm nghiệm chất lượng của dược chất và thành phẩm, nên bản thân chất chuẩn cần được xác định đặc tính ở mức độ cao hơn so với các phép thử được quy định trong dược điển và thường đòi hỏi áp dụng nhiều kỹ thuật bổ trợ. Đánh giá liên phòng dùng đánh giá chất chuẩn thường áp dụng: (i) Nhiều phương pháp định tính bổ trợ như NMR, phân tích trình tự peptide, HPLC và phân tích amino acid; (ii) Nhiều phương pháp khác nhau để đánh giá tạp chất; (iii) Phương pháp khối lượng cân bằng (mass balance) để xác định giá trị định lượng, đảm bảo tất cả các thành phần như ion đối, dung môi tồn dư… được tính đến đầy đủ [13].
Sai số hay thiên lệch trong các phương pháp xác định hàm lượng hoặc biến đổi của chất chuẩn trong quá trình bảo quản đều có thể dẫn đến việc gán sai hàm lượng lọ chuẩn. Đánh giá liên phòng do USP hay các tổ chức thiết lập tiêu chuẩn khác có thể ghi nhận sự biến thiên phân tích và điều chỉnh các sai lệch giữa các phòng thí nghiệm trong việc xác lập giá trị cho chất chuẩn. Để giải quyết các vấn đề về độ ổn định, công thức và cấu trúc của chuẩn peptide được thiết kế để hỗ trợ việc bảo quản lâu dài, đồng thời thực hiện các nghiên cứu ổn định tăng tốc nhằm mô phỏng sự phân hủy theo thời gian. Ngoài ra, độ ổn định cần cũng được theo dõi theo thời gian thực nhằm xác nhận rằng chất chuẩn vẫn còn phù hợp sử dụng theo danh mục công bố [13].
Hội đồng Dược điển Hoa Kỳ đã xây dựng quy trình thiết lập và chiến lược kiểm nghiệm chuẩn peptide, tập trung vào chuẩn dạng đông khô giúp người dùng không cần xác định ion đối và độ ẩm tồn dư trước khi sử dụng. Những điểm cần lưu ý khi thiết lập chất chuẩn peptide, cùng với quy trình xác định đặc tính và kiểm nghiệm nguyên liệu để thiết lập chất chuẩn được thể hiện ở Bảng 6 [13].
Bảng 6. Hướng dẫn các bước thiết lập chất chuẩn peptide của USP [13]
Bước | Nội dung | Nhận xét |
1. Kiểm nghiệm nguyên liệu thiết lập chuẩn | * Quy trình của USP áp dụng được cho chuẩn peptide có độ dài từ 8 tới 39 AA; cấu trúc mạch thẳng hoặc vòng; không chứa hoặc có chứa D-acid amin. Nguyên liệu để thiết lập chuẩn có dạng bột rắn, số lượng lớn.
|
|
2. Chiết rót chuẩn vào lọ và đông khô |
| |
3. Kiểm tra tính chất vật lý các lọ chuẩn |
| |
4. Thử nghiệm độ ổn định tăng tốc (ATD) |
|
|
5. Xác định hàm lượng peptide trong mỗi lọ chuẩn dựa trên đánh giá liên phòng |
|
|
USP áp dụng tính khoa học nghiêm ngặt và các thực hành tốt nhất trong việc thiết lập chất chuẩn theo dược điển – những yếu tố đóng vai trò quan trọng trong việc đảm bảo chất lượng của thuốc. Danh sách chất chuẩn peptide của USP phục vụ kiểm nghiệm và nghiên cứu được trình bày ở Bảng 7.
Bảng 7. Danh sách chuẩn peptide của USP [11]
Chuẩn peptide | Tạp đối chiếu tương ứng |
| Chuẩn peptide | Tạp đối chiếu tương ứng |
*Octreotide RS | [Lys(Ac)]5-Octreotide |
| *Exenatide | [Asp]28-Exenatide |
Parallel Dimer-Octreotide |
| Amidated Exenatide (C-terminal) | ||
Anti-parallel Dimer-Octreotide |
| *Glucagon | Des-Thr-Glucagon | |
[O1(Ac)]8-Octreotide |
| Met(O)-Glucagon | ||
[Phe(Ac)]1-Octreotide |
| Glu 24-Glucagon | ||
N-Acetyl-Lys-Octreotide TFA |
| Glu 3-Glucagon | ||
N-Acetyl-Phe-Octreotide TFA |
| Glu 20-Glucagon | ||
*Teriparatide RS | [MetO8]-Teriparatide |
| *Vasopressin | Glu 4-Vasopressin |
[MetO18]-Teriparatide |
| Parallel Dimer-Vasopressin | ||
[Met+O8,18]-Teriparatide |
| Anti-parallel Dimer-Vasopressin | ||
*Leuprolide RS | [Pro(Ac)]1-Leuprolide |
| Asp 5-Vasopressin | |
[D-His]-Leuprolide |
| *Desmopressin | Di-Me-Gly-Desmopressin | |
[L-Leu]6-Leuprolide |
| *Calcitonin Salmon | Glu-20 Calcitonin Salmon | |
[D-Ser]-Leuprolide |
| Glu-14 Calcitonin Salmon | ||
[Ser(Ac)]4-Leuprolide |
| Calcitonin Dimer Parallel | ||
*Oxytocin RS | [Cys(Ac)]1-Oxytocin |
| Ser (Ac)5-Calcitonin | |
[Asp]5-Oxytocin |
| Triple-Sulfate Calcitonin | ||
[Glu]4-Oxytocin |
| D-Leu(9) Calcitonin | ||
D-[Asp]5-Oxytocin |
| Des-Tyr(22) Calcitonin | ||
Parallel Dimer-Oxytocin |
| *Bivalirudin | [12-20] Bivalirudin | |
Anti-parallel Dimer-Oxytocin |
| [1-11] Bivalirudin | ||
|
|
| *Cosyntropin Acetate | Met(O) cosyntropin |
*Có chuyên luận USP tương ứng
Sự tăng trưởng nhanh chóng của thị trường peptide trị liệu trong những năm gần đây phản ánh tiềm năng lớn của nhóm thuốc này trong điều trị các bệnh lý phức tạp như ung thư, rối loạn chuyển hóa, bệnh hiếm và miễn dịch. Tuy nhiên, song hành với sự phát triển đó là nhu cầu ngày càng cao về các chiến lược kiểm soát chất lượng chặt chẽ và toàn diện. Chất lượng của peptide trị liệu phụ thuộc vào việc thiết lập tiêu chuẩn rõ ràng, sử dụng chất chuẩn phù hợp, và áp dụng các phương pháp phân tích chính xác. Sự phức tạp trong cấu trúc và quy trình sản xuất peptide đòi hỏi sự tuân thủ nghiêm ngặt các hướng dẫn từ các đơn vị như ICH, EMA, FDA hay USP. Để đảm bảo an toàn và hiệu quả cho người bệnh, các bên liên quan—bao gồm nhà sản xuất, phòng kiểm nghiệm, và cơ quan quản lý—cần hợp tác chặt chẽ trong việc áp dụng tiêu chuẩn quốc tế và cải tiến phương pháp đánh giá chất lượng peptide. Điều này đặc biệt quan trọng khi lĩnh vực peptide trị liệu đang ngày càng mở rộng với các sản phẩm đa dạng và công nghệ sản xuất tiên tiến.
Tài liệu tham khảo
Cơ quan chủ quản: Viện Kiểm nghiệm thuốc thành phố Hồ Chí Minh
Giấy phép hoạt động: số ... /GP-BVHTTDL ngày .../.../...
Cơ quan cấp phép: Bộ Văn hóa, Thể thao và Du lịch
Copyright @2026 Viện Kiểm nghiệm thuốc TP. HCM
Địa chỉ: 200 Cô Bắc, P. Cầu Ông Lãnh, TP.HCM
Email: journal@vjtst.vn
Website: www.vjtst.vn
Tổng biên tập: ..............................................của Widget đoạn văn. Bạn có thể tự sửa nội dung này trong phần tác vụ khác củaidget hoặc thiết lập dữ liệu động tùy theo nhu cầu.